zertifiziert nach DKG und ISO 9001:2015
 Leitbild | Organisation | Selbsthilfe | Akkreditierung | Kooperationspartner*innen
Leitbild | Organisation | Selbsthilfe | Akkreditierung | Kooperationspartner*innen
Unser Leitbild
Das Zentrum für Zelltherapie und Stammzelltransplantation Bonn (ZZSB) folgt dem Leitsatz des CIO:
"Gemeinsam gegen den Krebs. Gemeinsam für das Leben."
Im Zentrum für Zelltherapie und Stammzelltransplantation Bonn werden unter dem Direktorium von Herrn Prof. Peter Brossart (MED III) und Herrn Prof. Johannes Oldenburg (IHT) und der ärztlichen Leitung von Herrn Dr. Tobias Holderried modernste zelluläre Immuntherapien wie die CAR-T-Zelltherapien sowie autologe und allogene Stammzelltransplantationen durchgeführt. Darüber hinaus wird in klinischen Studien die Wirksamkeit zielgerichteter Zelltherapien bei soliden Tumoren untersucht. Durch die Teilnahme an multizentrischen internationalen klinischen Studien haben unsere Patient*innen die Möglichkeit, höchst innovative Behandlungsansätze zu erhalten, mit den Zielen, die Ansprechraten und -dauer zu verbessern sowie mögliche Komplikationen zu reduzieren bzw. zu behandeln. Detaillierte Angaben zu unseren klinischen Studien finden Sie in der Studienübersicht.
Der wissenschaftliche Fokus liegt neben klinischen Studien in der intensiven translationalen Erforschung zellulärer und humoraler immunregulatorischer Mechanismen, welche im Rahmen einer Stammzelltransplantation oder CAR-T-Zelltherapie die Immunreaktion beeinflussen.
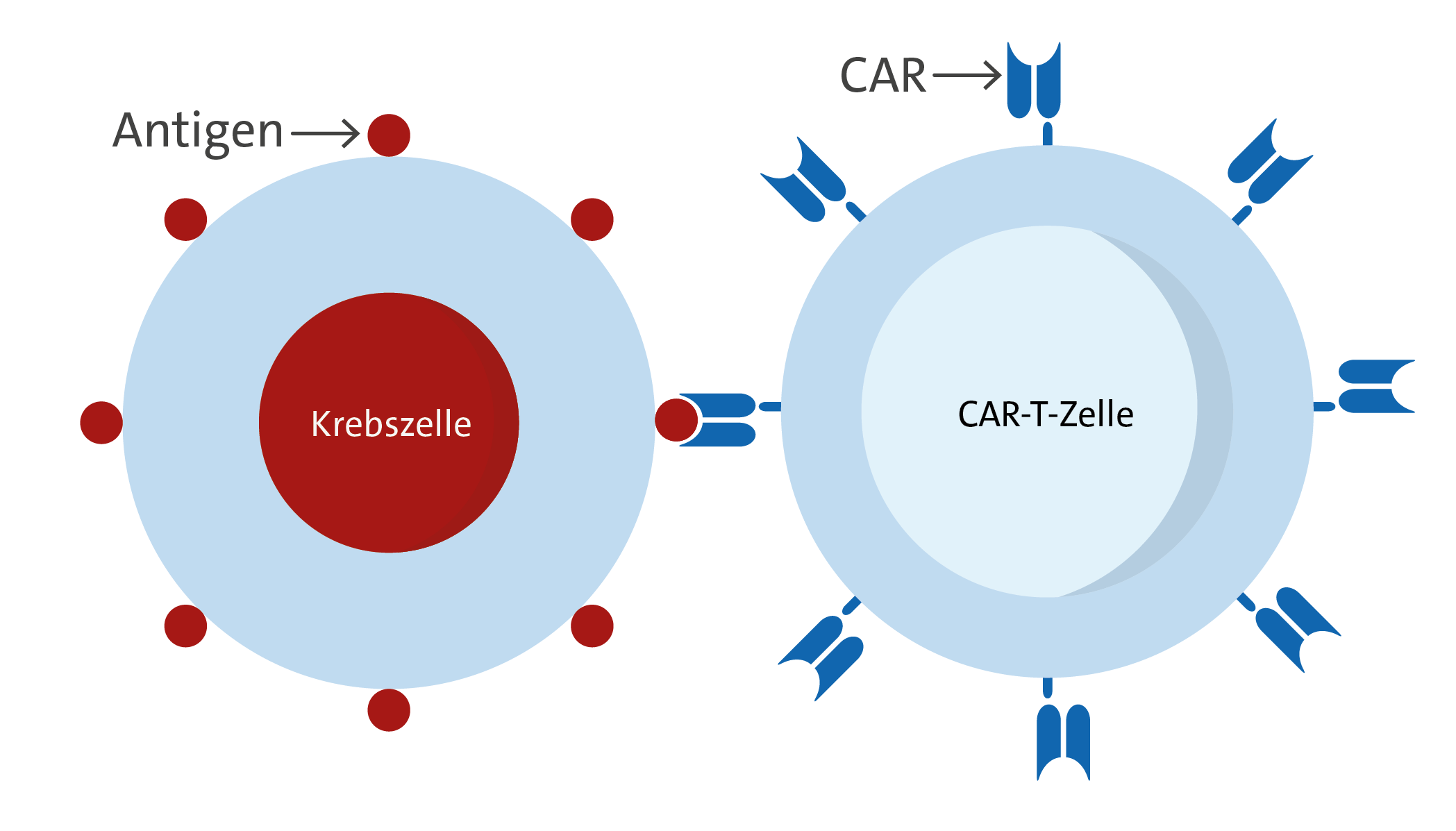
› CAR-T-Zelltherapie
- Diffus großzelliges B-Zell Lymphom
- Primär mediastinales B-Zell Lymphom
- Mantelzelllymphom
- Multiples Myelom
- Akute Lymphatische Leukämie
- Follikuläres Lymphom
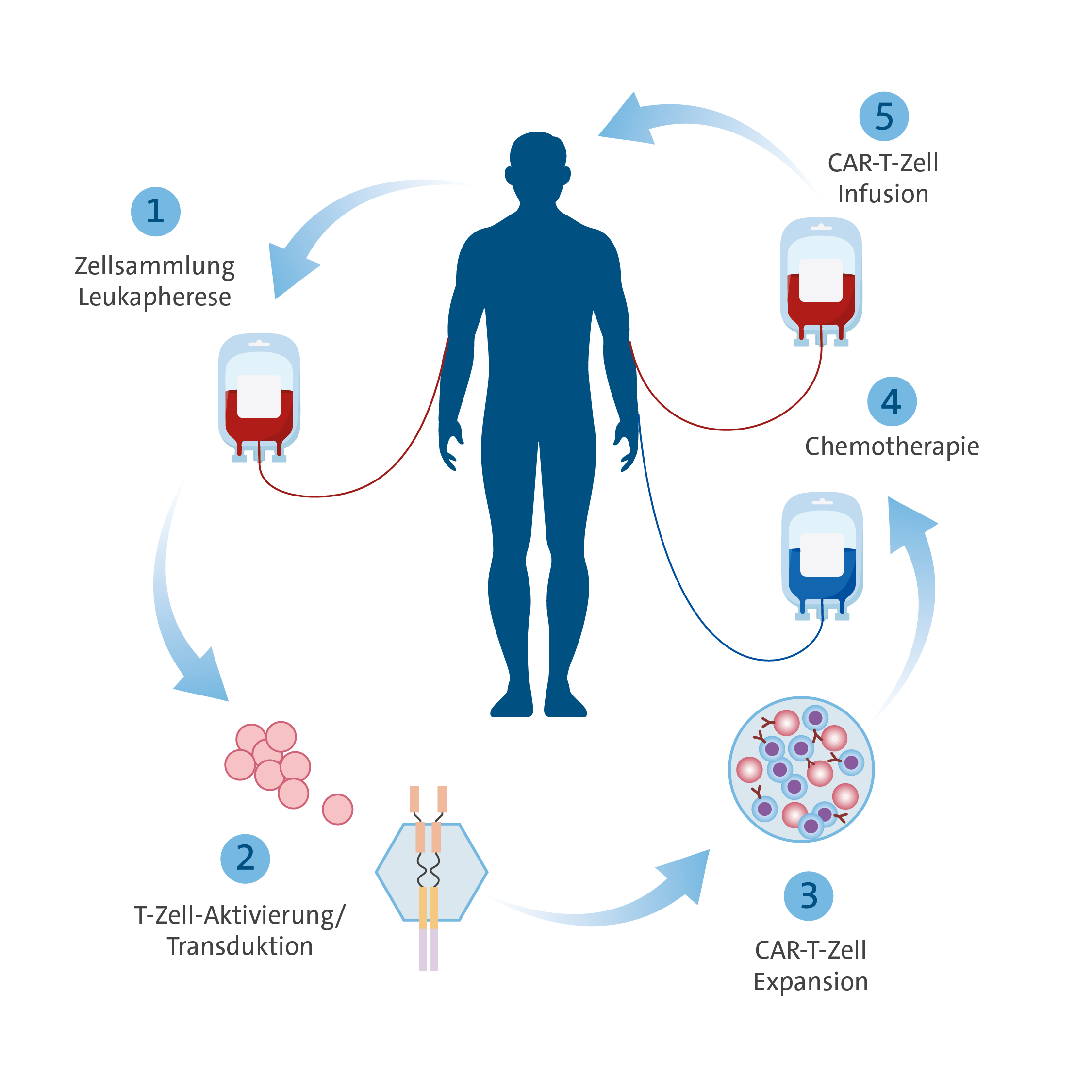
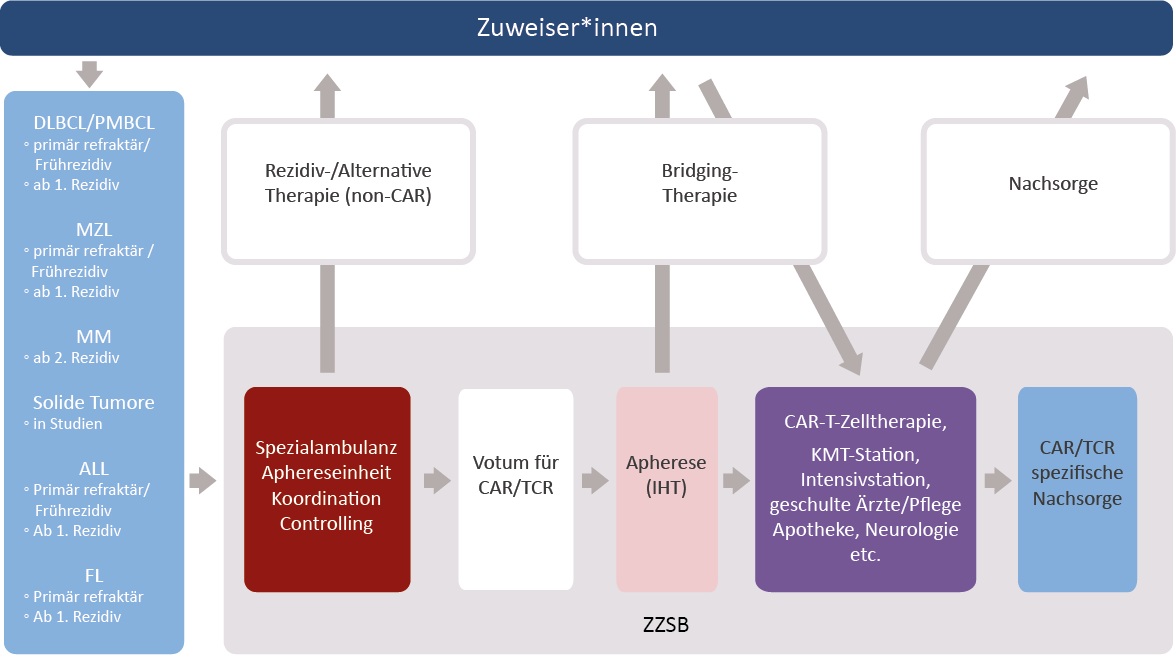
Auch wenn es sich bei den CAR-T-Zellen definitionsgemäß um Arzneimittel handelt, handelt es sich hierbei um „lebende“ Medikamente, deren Herstellung und Applikation komplexe Abläufe beinhaltet und deren Verabreichung daher nur in spezialisierten Zentren erfolgen darf. Der Ablauf einer CAR-T-Zelltherapie ist in der Regel wie im folgenden Schema dargestellt:
Durchführung der CAR-Therapie:
› Allogene Stammzelltransplantation
- akute Leukämien (AML / ALL)
- Myelodysplastisches Syndrom (MDS)
- Myeloproliferative Neoplasien (MPN)
- Multiples Myelom
- Non-Hodgkin Lymphome
- schwere aplastische Anämie
Mögliche Spender:
- Voll-passende Familienspender*innen
- Voll-passende Fremdspender*innen
- Nicht-voll-passende („mismatch“) Fremdspender*innen
- Halb-passende („haploidenter“) Familienspender*innen
Durchführung der allogenen Stammzelltransplantation:
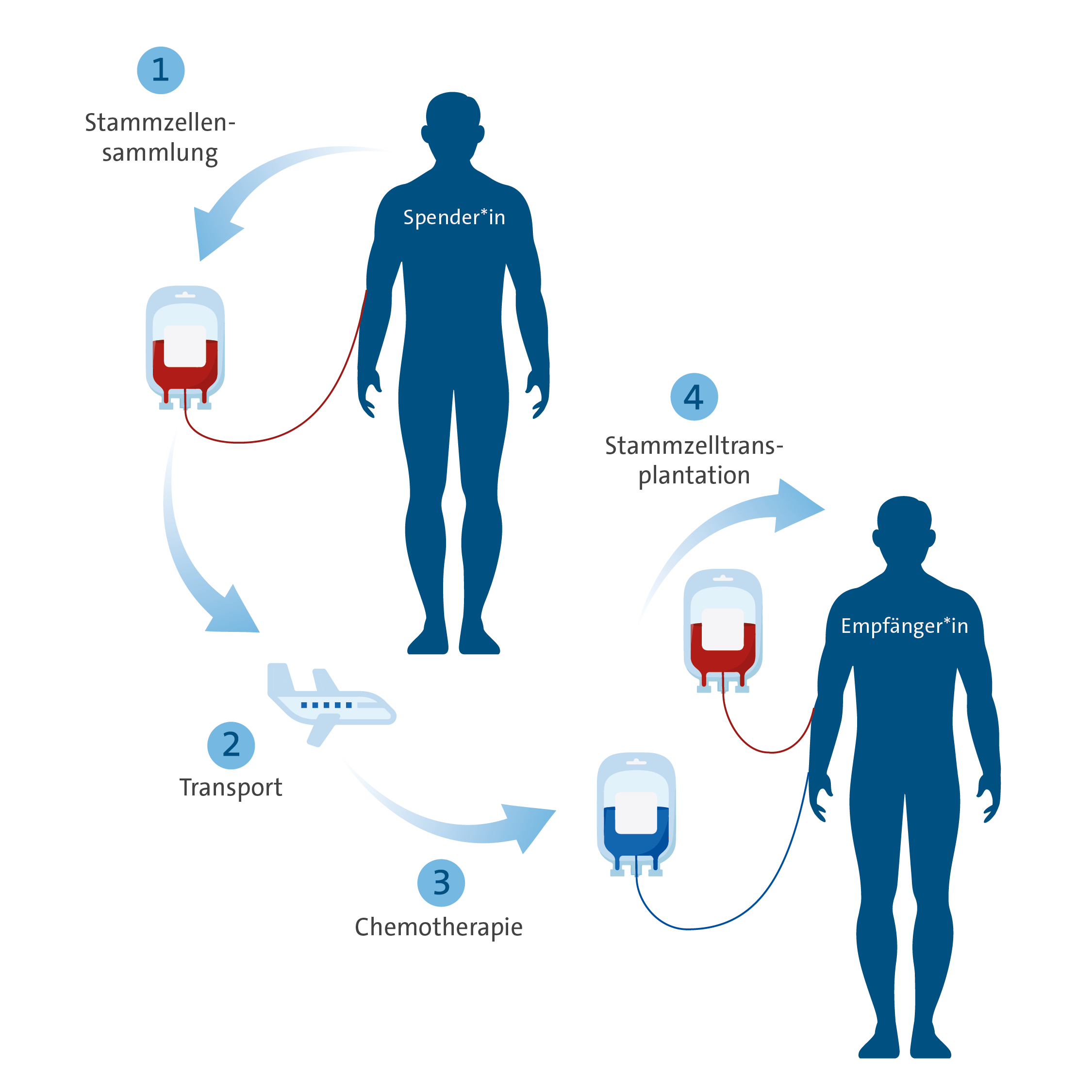
- Myeloablative Konditionierung
- Nicht-myeloablative Konditionierung mit reduzierter Toxizität, welche eine allogene Stammzelltransplantation auch bei Patient*innen über 70 Jahren ermöglicht
› Autologe Stammzelltransplantation
- Multiples Myelom
- hoch- und niedrigmalignen Non-Hodgkin-Lymphome
- Morbus Hodgkin
- ausgewählten soliden Tumorerkrankungen (Sarkomen)
Durchführung der autologen Stammzelltranspantation:
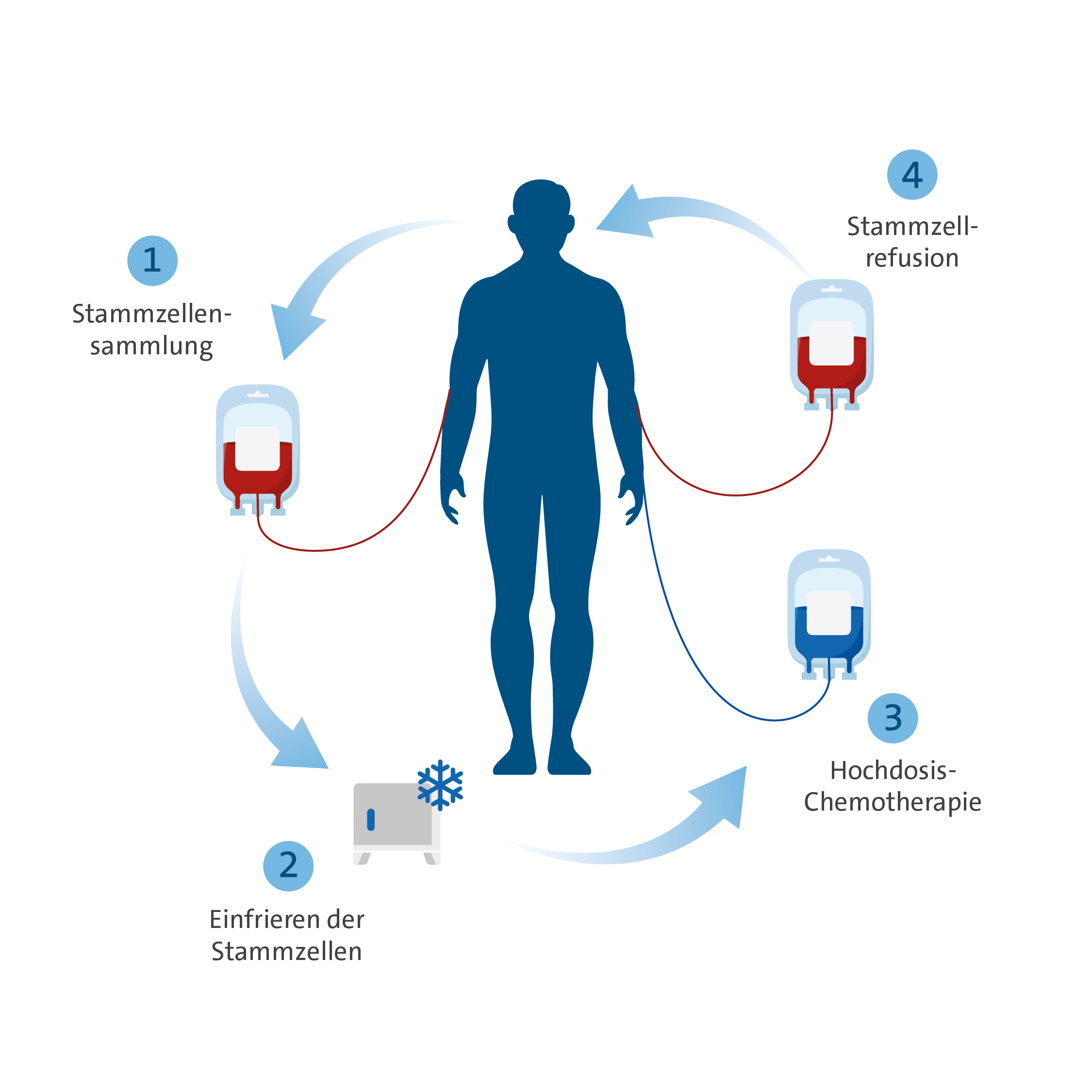
› Studien
Durch die Teilnahme an multizentrischen internationalen klinischen Studien haben unsere Patient*innen die Möglichkeit, höchst innovative Behandlungsansätze zu erhalten, mit den Zielen, die Ansprechraten und -dauer zu verbessern sowie mögliche Komplikationen zu reduzieren bzw. zu behandeln.
Hier finden Sie eine Auflistung unserer klinischen Studien:
- Titel: Phase 1 Study Evaluating Genetically Modified Autologous T Cells Expressing a T-cell Receptor Recognizing a Cancer/Germline Antigen in Patients With Recurrent and/or Refractory Solid Tumors (ACTengine® IMA201-101)
- Behandlung von Patiet*innen mit soliden Tumoren mit genetisch veränderten, patient*inneneigenen T-Zellen, die einen tumor-spezifischen T-Zellrezeptor tragen (Phase I Prüfung)
- Ziel: Inzidenz von unerwünschten Ereignissen und Dosisfindung.
- Clinical Trials: NCT03247309
- Aktuell keine Rekrutierung
- Titel: Phase 1 Study Evaluating Genetically Modified Autologous T Cells Expressing a T-cell Receptor Recognizing a Cancer/Germline Antigen in Patients With Recurrent and/or Refractory Solid Tumors(ACTengine® IMA202-101)
- Behandlung von Patienten mit soliden Tumoren mit genetisch veränderten, patienteneigenen T-Zellen, die einen tumor-spezifischen T-Zellrezeptor tragen (Phase I Prüfung)
- Ziel: Inzidenz von unerwünschten Ereignissen und Dosisfindung
- Clinical Trials: NCT03441100
- Aktuell keine Rekrutierung
- Titel: Phase 1 Study Evaluating Genetically Modified Autologous T Cells Expressing a TCR Recognizing a Cancer/Germline Antigen as Monotherapy or in Combination With Nivolumab in Patients With Recurrent and/or Refractory Solid Tumors
- Behandlung von Patienten mit soliden Tumoren mit genetisch veränderten, patienteneigenen T-Zellen, die einen tumor-spezifischen T-Zellrezeptor tragen (Phase I Prüfung)
- Ziel: The study purpose is establish the safety and tolerability of IMA203 product in patients with solid tumors that express preferentially expressed antigen in melanoma (PRAME).
- Clinical Trials: NCT03686124
- Titel: A Randomized Controlled Trial Comparing Outcome After Hematopoietic Cell Transplantation From a Partially Matched Unrelated Versus Haploidentical Donor
- Randomisierte kontrollierte klinische Prüfung zum Vergleich der Blutstammzelltransplantation von partiell-passenden unverwandten Stammzellspendern mit haplo-identen verwandten Stammzellspendern
- Ziel: Gesamtüberleben.
- Clinical Trials: NCT03275636
- Titel: Primary Comparison of Liposomal Anthracycline Based Treatment Versus Conventional Care Strategies Before Allogeneic Stem Cell Transplantation in Patients With Higher Risk MDS and Oligoblastic AML
- Primärer Vergleich der Behandlung auf der Basis von Liposomalem Anthracyclin im Vergleich zu konventionellen Behandlungsstrategien vor der allogenen Stammzelltransplantation bei Patienten mit Hochrisiko MDS oder oligoblastischer AML - die PALOMA-Studie
- Ziel: Vergleich des ereignisfreien Überlebens (EFS) nach 2 Jahren von CPX-351 vs. CCR vor allogener Blutzelltransplantation (alloHCT) als Erstlinienbehandlung bei Patienten mit erhöhtem MDS-Risiko und oligoblastischer AML.
- Clinical Trials: NCT04061239
- Titel: A Randomised, Open-label, Multicentre, Phase 3 Trial of First-line Treatment With Mesenchymal Stromal Cells MC0518 Versus Best Available Therapy in Adult and Adolescent Subjects With Steroid-refractory Acute Graft-versus-host Disease After Allogeneic Haematopoietic Stem Cell Transplantation (IDUNN Trial)
- Eine randomisierte, offene multizentrische Phase-3-Studie zur Erstlinienbehandlung mit mesenchymalen Stromazellen MC0518 gegenüber der besten verfügbaren Therapie bei erwachsenen und jugendlichen Patienten mit steroidrefraktärer akuter Graft-versus-Host-Krankheit nach allogener hämatopetischer Stammzelltransplantation (IDUNN-Studie)
- Ziel: Nachweis der Überlegenheit von MC0518 im Vergleich zur zuerst eingesetzten besten verfügbaren Therapie (BAT) in Bezug auf die Gesamtansprechrate (ORR) bei erwachsenen und jugendlichen Patienten mit steroidrefraktärer akuter Transplantat-gegen-Wirt-Krankheit (SR-aGvHD) am Besuchertag 28.
- Clinical Trials: NCT04629833
Alle weiteren detaillierte Angaben entnehmen Sie bitte unserem CIO-Studienregister.
Medizinische Klinik und Poliklinik III – Innere Medizin mit den Schwerpunkten Onkologie, Hämatologie, Immunonkologie, Stammzelltransplantation und Rheumatologie

Dr. med. Tobias Holderried
Leiter des ZZSB (MED III)

Univ.-Prof. Dr. med. Annkristin Heine
Stellv. Leiterin des ZZSB (MED III)

Dr. med. Martin Schumacher
Stellv. Leiter des ZZSB (MED III)

Univ.-Prof. Dr. med. Peter Brossart
Direktor der Medizinischen Klinik und Poliklinik III – Innere Medizin mit den Schwerpunkten Onkologie, Hämatologie, Immunonkologie, Stammzelltransplantation und Rheumatologie
Institut für Experimentelle Hämatologie und Transfusionsmedizin

Univ.-Prof. Dr. med. Eva Bartok
Leiterin des ZZSB (IHT)

PD Dr. med. Vytautas Ivaskevicius
Leiter des ZZSB (IHT)

PD Dr. med. Dipl.-Kfm. Heiko Rühl
Leiter des ZZSB (IHT)

Univ.-Prof. Dr. med. Johannes Oldenburg
Direktor des Instituts für Experimentelle Hämatologie und Transfusionsmedizin
Organisation
Die Koordination
Tel.: +49 (0) 228 287-17166
…begleitet Sie und koordiniert Abläufe der Therapie
Die Station
Tel.: +49 (0) 228 287-17407
… betreut Sie während der Stammzelltransplantation / CAR-T-Zelltherapie.
Die Ambulanz
Tel.: +49 (0) 228 287-17158
+49 (0) 228 287-17168
… ist für die Betreuung vor und nach der Therapie für Sie verantwortlich.
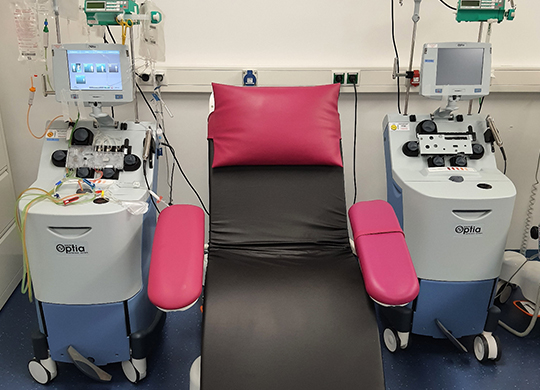
Die Leukapherese-Einheit
Tel.: +49 (0) 228 287-16714
…betreut Sie während der Zellsammlung
In der GMP-Einheit
Tel.: +49 (0) 228 287-15176
…werden Zelltherapeutika hergestellt und ihre Qualität überwacht

Die Studienzentrale der MED III
Tel.: +49 (0) 228 287-17236
... koordiniert die Durchführung von klinischen Studien.
Weitere Einheiten unseres Zentrums:
Das Zentrum für Stammzelltransplantation und Zelltherapie (ZZSB) des CIO Bonn arbeitet eng mit unterschiedlichen Kliniken und Abteilungen zusammen, wie beispielsweise mit:
- Psychoonkologie
- Ernährungsberatung
- Physiotherapie
- Entlassmanagement/Sozialdienst
- Leukämie-Initiative Bonn e.V.
Selbsthilfe
Das Zentrum für Stammzelltransplantation und Zelltherapie Bonn (ZZSB) arbeitet eng mit folgenden Selbsthilfegruppen und patient*innennahen Organisationen zusammen:
- KMT Selbsthilfegruppe der Leukämie - Initiative Bonn e.V.
- Leukämie-Initiative Bonn e.V.
- Weitere zentrale Kontaktstellen in der Region und einzelne Selbsthilfegruppen finden Sie hier.
- Die Deutsche Krebshilfe berät über das INFONETZ KREBS kostenfrei - telefonisch (+49 800 80 70 88 77) Erkrankte, Angehörige und Betroffene zu der Diagnose Krebs und hat spezielle Ratgeber herausgegeben:
Die › Blauen Ratgeber.
Alle 6 Monate treffen sich über 20 Gruppen zu einem gemeinsamen Runden Tisch im CIO Bonn, um den gegenseitigen Austausch zu fördern. Hieran nehmen auch Entitäten übergreifende Gruppen teil.
Akkreditierung und Einbindung in nationale/internationale Aktivitäten
Die Medizinischen Klinik III ist ein durch die European Group for Blood and Marrow Transplantation (EBMT) anerkanntes Zentrum für autologe und allogene Stammzelltransplantation und CAR-T-Zelltherapien. Dr. Holderried ist Mitglied des deutschen kooperativen Transplantations-Netzwerks. Zudem sind wir durch die ZKRD anerkannt und beziehen über die ZKRD Stammzellen oder Knochenmark für Fremdspender-Transplantationen. Die Ergebnisse der Transplantationen werden nationalen und internationalen Registern in formalisierter und anonymisierter Form übertragen.




Weitere Informationen zum PJ Wahltertial am CIO Bonn "Interdisziplinäre Onkologie" finden sie hier.
Materialien
Evaluationsbogen
"Welche onkologischen Qualitätsindikatoren sind am Wichtigsten bei der Behandlung einer Patientin?"
Hier gelangen Sie zum Evalustionsbogen

Logbuch
Hier gelangen Sie zu unserem digitalen Logbuch
Krebsbehandlung | Unterstützende Krebstherapien und Angebote | Krebsprävention | Krebsforschung
Was ist Krebs?
Krebs, auch bekannt als maligne Neubildung, ist eine Krankheit, bei der abnorme Zellen unkontrolliert im Körper wachsen. Diese Zellen können sich auf verschiedene Organe oder Gewebe ausbreiten und den normalen Betrieb des Körpers stören. Es gibt viele verschiedene Arten von Krebs, die in unseren Organkrebszentren spezifisch diagnostiziert und behandelt werden. Die Symptome von Krebs können je nach Art und Stadium variieren. Einige häufige Anzeichen sind ungewollter Gewichtsverlust, anhaltende Müdigkeit, Schmerzen und Veränderungen in der Haut. Es ist wichtig, keine Selbstdiagnosen zu stellen, sondern einen Arzt aufzusuchen. Dieser kann Symptome frühzeitig und sicher erkennen, um eine angemessene Behandlung zu ermöglichen.
Krebs ist eine komplexe und ernsthafte Erkrankung, die viel Aufmerksamkeit erfordert. Es ist wichtig, dass Menschen über die Risikofaktoren, Symptome und Behandlungsmöglichkeiten von Krebs informiert sind. Durch eine Kombination aus Prävention, Früherkennung, fortschrittlichen Behandlungen und einer gewissenhaften Krebsnachsorge können wir gemeinsam gegen den Krebs und gemeinsam für das Leben kämpfen.
Krebsbehandlung
Es gibt verschiedene Krebsbehandlungsmöglichkeiten, darunter Chirurgie, Strahlentherapie, Chemotherapie, Immuntherapie und zielgerichtete Therapien. Die Wahl der Behandlung hängt von der Art des Krebses, dem Stadium der Erkrankung und anderen individuellen Faktoren ab. Jeder Krebsfall ist einzigartig, daher wird die Behandlung individuell auf den Patienten abgestimmt. Eine umfassende Krebsbehandlung erfordert eine individuelle Herangehensweise, bei der verschiedene Therapien und Unterstützungsmaßnahmen kombiniert werden. Es ist wichtig, mit einem Onkologen zusammenzuarbeiten, um die besten Behandlungsoptionen zu identifizieren und eine optimale Versorgung zu gewährleisten.
Krebsbehandlungen können Nebenwirkungen haben. Diese variieren je nach Art der Behandlung und individuellen Faktoren. Zu den häufigen Nebenwirkungen gehören Müdigkeit, Übelkeit, Haarausfall und eine geschwächte Immunabwehr. Ihr Arzt wird Ihnen dabei helfen, mögliche Nebenwirkungen zu minimieren und mit ihnen umzugehen.
Wenn Sie auf der Suche nach Krebsbehandlungsmöglichkeiten sind, nehmen Sie Kontakt mit einem erfahrenen Onkologen auf, um eine fundierte Entscheidung zu treffen. Eine rechtzeitige Diagnose und angemessene Behandlung können die Chancen auf Genesung und ein gesundes Leben erhöhen. Hier finden SIe Ihr Organkrebszentrum, sowie die Sprechstunden
Chirurgie
Die chirurgische Entfernung von Tumoren ist oft eine der ersten Behandlungsmöglichkeiten. Je nach Krebsart und Stadium kann eine Operation allein oder in Kombination mit anderen Therapien eingesetzt werden.
Strahlentherapie
Bei der Strahlentherapie werden hochenergetische Strahlen verwendet, um Krebszellen abzutöten oder ihr Wachstum zu hemmen. Dieses Verfahren kann vor, während oder nach der Operation angewendet werden.
Chemotherapie
Die Chemotherapie nutzt Medikamente, um Krebszellen zu zerstören oder ihr Wachstum zu verlangsamen. Diese Medikamente können oral eingenommen oder intravenös verabreicht werden und wirken im gesamten Körper.
Immuntherapie
Die Immuntherapie zielt darauf ab, das Immunsystem des Körpers zu stärken, um Krebszellen besser zu erkennen und zu bekämpfen. Diese Behandlungsoption hat sich als besonders wirksam bei bestimmten Krebsarten wie Melanom, Lungenkrebs und Nierenkrebs erwiesen.
Zielgerichtete Therapien
Diese Behandlungen richten sich gezielt an bestimmte Moleküle oder Genmutationen, die für das Wachstum von Krebszellen verantwortlich sind. Zielgerichtete Therapien können die Nebenwirkungen im Vergleich zur Chemotherapie verringern und die Wirksamkeit der Behandlung verbessern.
Krebsnachsorge
Nach Abschluss der akuten Krebstherapie, ist die Nachsorge ein wichtiger Teil in der Krebsbehandlung. Regelmäßige Arztbesuche, Untersuchungen und bildgebende Verfahren werden durchgeführt, um den Erfolg der Behandlung zu überwachen, Rückfälle frühzeitig zu erkennen und weiterhin die bestmögliche Betreuung sicherzustellen.
Unterstützende Krebstherapien und Angebote
Neben den medizinischen Behandlungen in der Krebstherapie können auch unterstützende Maßnahmen eine wichtige Rolle spielen, um das Wohlbefinden während der Krebsbehandlung zu verbessern. Hier im CIO bieten wir folgende Supportiven Angebote an:
- Bewegung und Sport
- Entlassmanagement/Sozialdienst
- Ernährungstherapie,
- Familien-SCOUT (Unterstützungsangebot)
- Klinikseelsorge
- Komplementärmedizin
- Kunsttherapie
- Palliativmedizin,
- Patientenverfügung
- Psychoonkologie,
- Selbsthilfe.
Krebsprävention
Um das Risiko von Krebs zu verringern, ist es wichtig, einen gesunden Lebensstil zu pflegen. Dazu gehört regelmäßige körperliche Aktivität, eine ausgewogene Ernährung mit viel Obst und Gemüse sowie der Verzicht auf das Rauchen. Einige Krebsarten können auch durch Impfungen, wie z.B. den HPV-Impfstoff zur Vorbeugung von Gebärmutterhalskrebs, verhindert werden.
Krebsforschung
In der Forschung werden ständig Fortschritte gemacht, um bessere Behandlungsmethoden und Präventionsstrategien für Krebs zu entwickeln. Klinische Studien spielen eine wichtige Rolle bei der Erforschung neuer Ansätze und Medikamente. Durch solche Studien können Patienten Zugang zu experimentellen Behandlungen erhalten und gleichzeitig zur Weiterentwicklung der Krebsmedizin beitragen.
Tumorboards
Expertise und Entscheidungsfindung bei Krebsbehandlungen
Die Vorteile eines Tumorboards sind vielfältig. Sie ermöglichen eine umfassende Bewertung des individuellen Falls eines Patienten aus verschiedenen medizinischen Blickwinkeln. Dies führt zu fundierten Entscheidungen über die besten Behandlungsoptionen. Die Diskussionen im Tumorboard fördern den Informationsaustausch, die Zusammenarbeit und die kritische Überprüfung von diagnostischen Befunden und Therapieplänen. Dadurch können unnötige oder nicht geeignete Behandlungen vermieden und die Patientenversorgung insgesamt verbessert werden.
Die Bedeutung von Tumorboards erstreckt sich über die Diagnose hinaus bis zur Bewertung des Krankheitsverlaufs und zur Festlegung von Folgetherapien. Dies ist besonders wichtig bei komplexen oder fortgeschrittenen Krebserkrankungen, bei denen verschiedene Behandlungsmodalitäten miteinander kombiniert werden müssen.
Ein weiterer wichtiger Aspekt ist die Berücksichtigung der individuellen Bedürfnisse und Wünsche der Patienten. Tumorboards berücksichtigen die Lebensqualität und die Präferenzen der Patienten bei der Entwicklung von Behandlungsplänen, was zu einer patientenzentrierten Versorgung führt.
Unterkategorien
Das CIO Bonn ist Teil des Krebszentrums CIO Aachen Bonn Köln Düsseldorf.
Lesen Sie mehr darüber auf der gemeinsamen Webseite des Centrums für Integrierte Onkologie Aachen Bonn Köln Düsseldorf.